 Síguenos @ContraReplicaMX
Síguenos @ContraReplicaMX
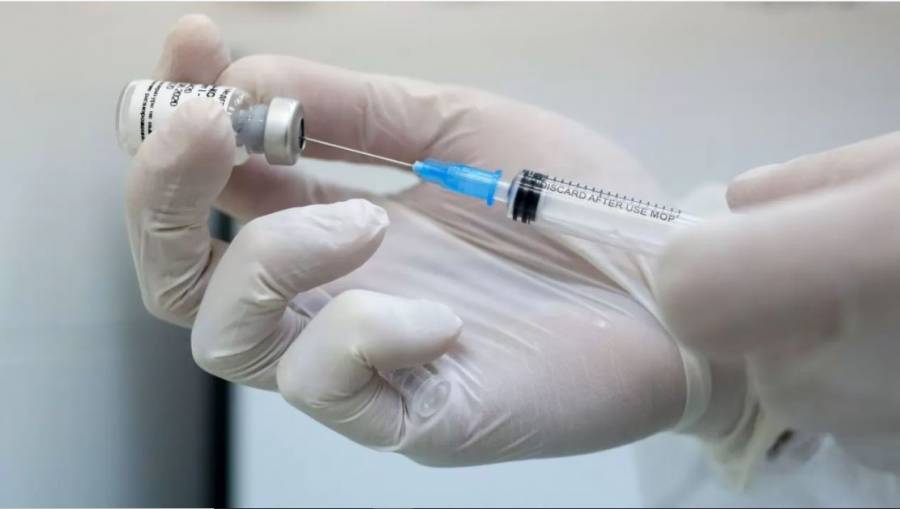
Pfizer busca uso de emergencia para su vacuna contra Covid-19
Global
Pfizer Inc anunció que solicitará la autorización para el uso de emergencia en Estados Unidos de su candidata a vacuna contra el Covid-19 alrededor de la tercera semana de noviembre, cuando espera haber alcanzado un objetivo clave sobre seguridad.
La farmacéutica estadounidense desarrolla la vacuna junto a la firma alemana BioNTech SE.
Por su parte, la Administración de Fármacos y Alimentos (FDA) de Estados Unidos destacó que requiere al menos dos meses de datos de seguridad antes de autorizar el uso de emergencia de una vacuna experimental contra el coronavirus.
A través de un comunicado, el presidente ejecutivo de la compañía, Albert Bourla, mencionó que, el ritmo actual de dosis y periodos en que se integran los voluntarios, Pfizer espera contar con los datos de seguridad en la tercera semana de noviembre.
Pfizer había dicho previamente que esperaba obtener los datos de sus ensayos clínicos de fase final en octubre.
Información de Agencias
Imagen de Twitter
Información de Agencias
Imagen de Twitter
Envíe un mensaje al numero 55 1140 9052 por WhatsApp con la palabra SUSCRIBIR para recibir las noticias más importantes.
SR/CR
Etiquetas
-
Coronavirus - Covid19 - Vacuna - Pfizer - Farmacéutica.
2024-04-17 - 20:12
2024-04-17 - 19:50
2024-04-17 - 19:46
2024-04-17 - 19:45
2024-04-17 - 19:44
2024-04-17 - 19:22
2024-04-17 - 18:57